Viết phương trình hóa học
Trong môn Hóa học, phương trình hóa học là ngôn ngữ đặc trưng giúp mô tả các phản ứng hóa học. Việc viết phương trình cân bằng hóa học không chỉ là kỹ năng cơ bản mà còn là nền tảng để bạn học tiếp các phần nâng cao. Nhiều bạn học sinh thường gặp khó khăn khi viết vì không biết bắt đầu từ đâu, hay lo lắng về việc cân bằng hệ số.
Thực chất, phương trình hóa học giống như một “ câu chuyện” được kể bằng ký hiệu hóa học. Nó cho thấy chất nào tham gia, chất nào sinh ra, và phản ứng xảy ra theo tỉ lệ như thế nào. Nếu không có phương trình, chúng ta khó có thể hình dung rõ ràng sự biến đổi từ chất này sang chất khác.
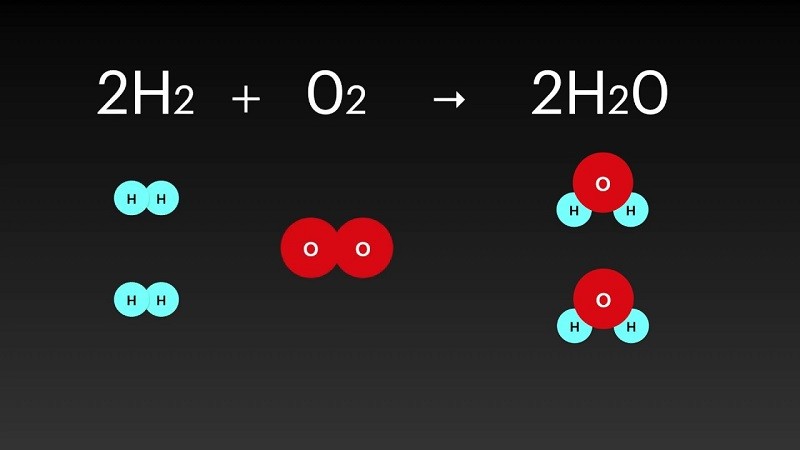
Ví dụ, thay vì diễn đạt dài dòng rằng “ khí hiđro phản ứng với khí oxi tạo ra nước” , ta chỉ cần viết gọn gàng: 2H2+O2 → 2H2O. Đây chính là sức mạnh của phương trình hóa học: ngắn gọn nhưng đầy đủ ý nghĩa.
Tầm quan trọng của việc viết phương trình cân bằng hóa học
Biết cách viết phương trình hóa học là kỹ năng bắt buộc nếu bạn muốn học giỏi môn Hóa. Nó giúp bạn:
Ghi nhớ và hiểu bản chất các phản ứng.
Dễ dàng tính toán theo công thức hóa học.
Vận dụng vào giải bài tập thực hành, từ cơ bản đến nâng cao.
Ngoài ra, phương trình hóa học còn là “ chìa khóa” để bạn tiếp cận các ngành liên quan như y dược, kỹ thuật, môi trường, sinh học phân tử.
Cách viết phương trình phản ứng hiđro và oxiĐể viết một phương trình hóa học chuẩn, bạn cần nắm rõ các thành phần cơ bản và những quy tắc đi kèm.
Thành phần của phương trình hóa học
Một phương trình hóa học hoàn chỉnh thường có ba phần: chất phản ứng, mũi tên phản ứng và sản phẩm. Chất phản ứng đặt bên trái, sản phẩm đặt bên phải, còn mũi tên biểu thị chiều của phản ứng.
Ví dụ: NaOH +HCl → NaCl+H2O
Trong phương trình trên, NaOH và HCl là chất phản ứng; NaCl và H2O là sản phẩm; còn dấu mũi tên thể hiện sự biến đổi từ trái sang phải.
Nguyên tắc cân bằng phương trình
Một trong những bước quan trọng khi viết phương trình cân bằng hóa học là cân bằng. Nguyên tắc chính là số nguyên tử của mỗi nguyên tố ở hai vế phải bằng nhau.
Ví dụ:
H2+O2 → H2O
Nếu viết như trên, ta thấy vế trái có 2 nguyên tử H và 2 nguyên tử O, trong khi vế phải chỉ có 2 nguyên tử H và 1 nguyên tử O. Để cân bằng, ta thêm hệ số:
2H2+O2 → 2H2O
Khi đó, số nguyên tử ở hai vế đã bằng nhau.
Một số quy tắc cần nhớ
Không được thay đổi chỉ số trong công thức hóa học của chất, chỉ được thêm hệ số trước công thức.
Luôn kiểm tra lại số nguyên tử của từng nguyên tố sau khi cân bằng.
Hệ số trong phương trình hóa học phải là số nguyên nhỏ nhất có thể.

Phản ứng kẽm với axit clohidricNhiều bạn học sinh thường hỏi: “ Làm thế nào để viết phương trình hóa học nhanh và chính xác?” Câu trả lời nằm ở việc nắm vững quy trình từng bước.
Bước 1: Xác định chất tham gia và sản phẩm
Trước tiên, bạn cần biết phản ứng hóa học đang diễn ra giữa những chất nào. Điều này dựa vào lý thuyết, kinh nghiệm hoặc yêu cầu của đề bài.
Ví dụ: Khi cho kẽm phản ứng với axit clohidric, ta dự đoán sản phẩm gồm muối ZnCl2 và khí H2.
Bước 2: Viết sơ đồ phản ứng
Tiếp theo, bạn viết sơ đồ gồm chất phản ứng và sản phẩm chưa cân bằng:
Zn+HCl → ZnCl2+H2
Bước 3: Cân bằng phương trình
Sau đó, tiến hành cân bằng:
Zn+2HCl → ZnCl2+H2
Khi cân bằng xong, bạn nên kiểm tra lại từng nguyên tố.
Bước 4: Hoàn thiện phương trình
Cuối cùng, viết phương trình đầy đủ, có thể thêm điều kiện phản ứng (nhiệt độ, xúc tác, trạng thái chất). Ví dụ:
Zn+2HCl (dd) → ZnCl2 (dd)+H2 (khí)

Phản ứng phân hủy canxi cacbonat khi nung nóngĐể hiểu rõ hơn, chúng ta hãy cùng đi qua một số ví dụ cụ thể.
Phản ứng oxi hóa – khử
Ví dụ: Cho Fe tác dụng với O2 tạo thành Fe2O3.
Sơ đồ: Fe+ O2 → Fe2O3
Cân bằng: 4Fe+3O2 → 2Fe2O3
Phản ứng axit – bazơ
Ví dụ: H2SO4 tác dụng với NaOH.
Sơ đồ: H2SO4 +NaOH → Na2SO4+H2O
Cân bằng: H2SO4+2NaOH → Na2SO4+2H2O
Phản ứng phân hủy
Ví dụ: Sự phân hủy của CaCO3 khi nung nóng.
Sơ đồ: CaCO3 → CaO+CO2
Phương trình: CaCO3 (r) → CaO (r)+CO2 (khí)
Phản ứng thế
Ví dụ: Cl2 tác dụng với NaBr.
Sơ đồ: Cl2+ NaBr → NaCl+Br2
Cân bằng: Cl2+2NaBr → 2NaCl+Br2
Để viết phương trình cân bằng hóa học chính xác, bạn cần thường xuyên luyện tập. Ngoài việc nhớ công thức hóa học của các chất, bạn còn cần nắm rõ tính chất hóa học của từng loại hợp chất. Chẳng hạn, kim loại kiềm tác dụng mạnh với nước, axit tác dụng với bazơ tạo muối và nước, hay phản ứng oxi hóa – khử thường kèm theo sự thay đổi số oxi hóa.
Một lưu ý khác là không phải phản ứng nào cũng xảy ra trong điều kiện bình thường. Có những phản ứng cần nhiệt độ cao, xúc tác hoặc dung môi thích hợp. Khi viết phương trình, nếu biết điều kiện, bạn nên ghi kèm để phương trình chính xác và đầy đủ.
Ngoài ra, trong các kỳ thi, nhiều bài tập yêu cầu viết phương trình cân bằng hóa học minh họa cho nhận xét. Vì vậy, bạn cần luyện tập nhiều dạng khác nhau để có phản xạ nhanh, tránh bỏ sót ý.
Qua bài viết này, bạn đã nắm được cách viết phương trình hóa học từ cơ bản đến minh họa cụ thể. Đây là kỹ năng quan trọng giúp bạn học tốt môn Hóa, cũng như là công cụ không thể thiếu trong nghiên cứu khoa học và đời sống. Hãy luyện tập thường xuyên để viết phương trình nhanh chóng, chính xác, từ đó nâng cao hiệu quả học tập và khả năng tư duy logic.