Bảng tuần hoàn nguyên tố hóa học
Trong Hóa học, bảng tuần hoàn nguyên tố hóa học là bảng sắp xếp các nguyên tố theo số hiệu nguyên tử tăng dần, đồng thời thể hiện quy luật biến đổi tuần hoàn về tính chất của chúng.
Hiểu đơn giản
- Mỗi nguyên tố chiếm một vị trí riêng trong bảng
- Các nguyên tố có tính chất giống nhau sẽ được xếp cùng một nhóm
- Khi đi từ trái sang phải hoặc từ trên xuống dưới, tính chất thay đổi theo quy luật
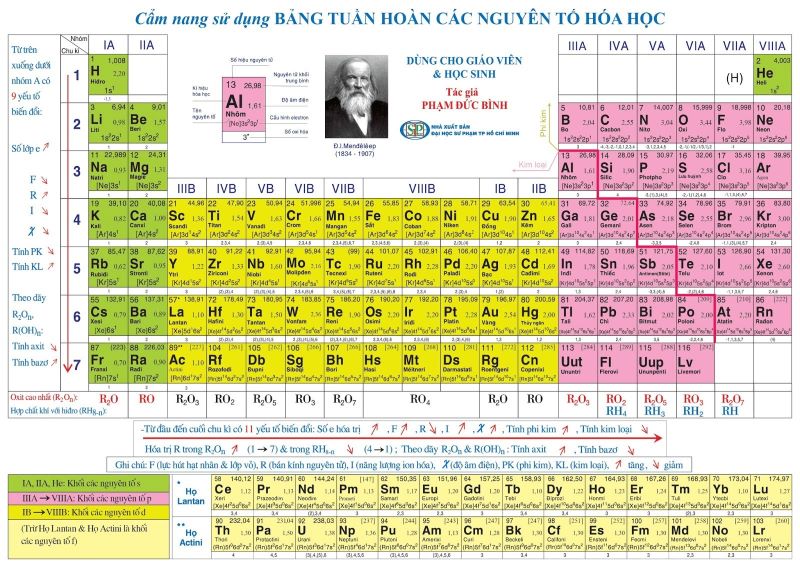
Bảng tuần hoàn nguyên tố Vai trò của bảng tuần hoàn
Bảng tuần hoàn không chỉ để tra cứu mà còn giúp bạn:
- Xác định nhanh thông tin của nguyên tố
- Dự đoán tính chất hóa học
- So sánh các nguyên tố với nhau
- Giải bài tập nhanh hơn
Ví dụ dễ hiểu
Natri (Na) và Kali (K) cùng một nhóm → đều là kim loại hoạt động mạnh
Oxi (O) và Lưu huỳnh (S) cùng nhóm → có nhiều tính chất tương tự
→ Nhìn vào vị trí là có thể đoán được phần nào tính chất của nguyên tố.
Bảng tuần hoàn được chia thành nhiều phần. Hiểu rõ cấu tạo sẽ giúp bạn đọc bảng nhanh và chính xác hơn.
Ô nguyên tố
Mỗi nguyên tố trong bảng nằm trong một “ ô” riêng, chứa các thông tin cơ bản:
- Số hiệu nguyên tử (Z): số proton trong hạt nhân
- Ký hiệu hóa học: viết tắt của nguyên tố (H, O, Na, … )
- Nguyên tử khối: khối lượng trung bình của nguyên tử
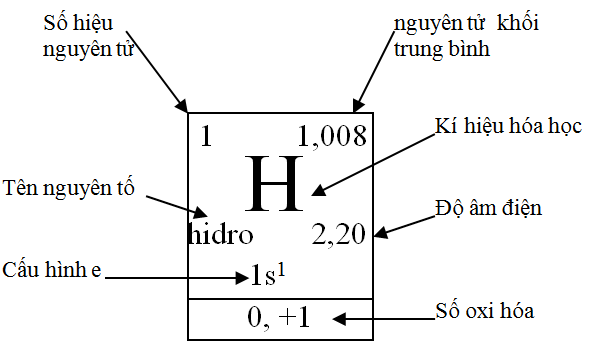
Cấu tạo Ô nguyên tố
Chu kỳ
Chu kỳ là hàng ngang trong bảng tuần hoàn
Hiện có 7 chu kỳ
Đặc điểm:
Số nguyên tử tăng dần từ trái sang phải
Tính chất thay đổi dần theo chiều ngang
Ví dụ:
Chu kỳ 2: Li, Be, B, C, N, O, F, Ne
Nhóm nguyên tố
Nhóm là cột dọc trong bảng
Các nguyên tố trong cùng nhóm có tính chất gần giống nhau
Có thể phân chia:
- Nhóm chính (A)
- Nhóm phụ (B) hoặc nguyên tố chuyển tiếp
Đặc điểm của nhóm
Cùng số electron lớp ngoài cùng
Tính chất hóa học tương tự
Ví dụ:
Nhóm 1: kim loại kiềm (Na, K, … )
Nhóm 17: halogen (F, Cl, … )
Nhóm 18: khí hiếm (He, Ne, … )
Cách ghi nhớ nhanh cấu tạo
Hàng ngang → chu kỳ
Cột dọc → nhóm
Mỗi ô → 1 nguyên tố
Khi đã hiểu cấu tạo, việc quan trọng tiếp theo là biết cách đọc thông tin từ bảng nguyên tố hóa học một cách nhanh và chính xác.
Cách xác định vị trí nguyên tố
Mỗi nguyên tố được xác định bởi:
- Chu kỳ (hàng ngang) → cho biết số lớp electron
- Nhóm (cột dọc) → cho biết số electron lớp ngoài cùng
Ví dụ:
Nguyên tố Na (Natri)
Chu kỳ 3 → có 3 lớp electron
Nhóm 1 → có 1 electron lớp ngoài cùng
Cách đọc thông tin trong ô nguyên tố
Một ô nguyên tố thường có các thông tin:
- Số hiệu nguyên tử (Z)
- Ký hiệu hóa học
- Nguyên tử khối
Ví dụ với Oxi (O):
Z=8 → có 8 proton
Nguyên tử khối ≈ 16
Ký hiệu: O
Ý nghĩa khi đọc bảng
Khi nhìn vào vị trí, bạn có thể suy ra:
- Nguyên tố thuộc kim loại hay phi kim
- Mức độ hoạt động hóa học
- Khả năng nhận hoặc nhường electron
Cách đọc nhanh trong bài tập
Nhìn nhóm → đoán tính chất
Nhìn chu kỳ → đoán cấu trúc electron
So sánh vị trí → suy ra nguyên tố mạnh/yếu hơn
Trong bảng tuần hoàn nguyên tố hóa học, các nguyên tố được chia thành nhiều nhóm dựa trên tính chất.
Kim loại
Đặc điểm:
- Dẫn điện, dẫn nhiệt tốt
- Dễ mất electron
- Thường nằm bên trái bảng
Ví dụ:
Na, K, Fe, Al

Các nhóm nguyên tố trong bảng tuần hoànPhi kim
Đặc điểm:
- Không dẫn điện
- Dễ nhận electron
- Thường nằm bên phải bảng
Ví dụ:
O, N, Cl, S
Khí hiếm
Đặc điểm:
- Rất ít phản ứng hóa học
- Có cấu hình electron bền
- Nằm ở nhóm cuối cùng (nhóm 18)
Ví dụ:
He, Ne, Ar
Nguyên tố chuyển tiếp
Đặc điểm:
- Nằm ở giữa bảng
- Có nhiều mức oxi hóa
- Tính chất phức tạp hơn
Ví dụ:
Fe, Cu, Zn
Cách phân biệt nhanh
- Bên trái → kim loại
- Bên phải → phi kim
- Cột cuối → khí hiếm
- Ở giữa → nguyên tố chuyển tiếp
Trong Hóa học, vị trí của nguyên tố trong bảng tuần hoàn nguyên tố hóa học giúp dự đoán nhiều tính chất quan trọng.
Xu hướng theo chu kỳ (từ trái sang phải)
- Bán kính nguyên tử: giảm dần
- Độ âm điện: tăng dần
- Tính kim loại: giảm
- Tính phi kim: tăng
Xu hướng theo nhóm (từ trên xuống dưới)
- Bán kính nguyên tử: tăng dần
- Độ âm điện: giảm dần
- Tính kim loại: tăng
- Tính phi kim: giảm
Ý nghĩa khi làm bài tập
- Nguyên tố càng “ bên phải, phía trên” → càng mạnh về phi kim
- Nguyên tố càng “ bên trái, phía dưới” → càng mạnh về kim loại
Mẹo 1: Nhớ theo vị trí
- Trái → kim loại
- Phải → phi kim
- Cuối bảng → khí hiếm
Mẹo 2: Nhớ theo chu kỳ
- Đi ngang → tính chất thay đổi dần
- Số lớp electron tăng theo chu kỳ
Mẹo 3: Nhớ theo nhóm
- Cùng nhóm → tính chất giống nhau
- Số electron lớp ngoài cùng giống nhau
Mẹo 4: Học theo cụm
Thay vì học từng nguyên tố, hãy học theo nhóm:
- Nhóm kim loại kiềm
- Nhóm halogen
- Nhóm khí hiếm
Bài 1
Nguyên tố Na thuộc chu kỳ mấy, nhóm mấy?
Đáp án:
Chu kỳ 3, nhóm 1
Bài 2
Nguyên tố nào sau đây là phi kim: Na, O, Fe?
Đáp án:
O
Bài 3
Nguyên tố nào có bán kính lớn hơn: Na hay K?
Đáp án:
K (vì nằm dưới Na trong cùng nhóm)
Bài 4
Trong các nguyên tố sau, nguyên tố nào có độ âm điện lớn nhất: F, Cl, Br?
Đáp án:
F (nằm trên cùng trong nhóm)
Bài 5
Nguyên tố nào thuộc nhóm khí hiếm?
Đáp án:
He, Ne, Ar
Có cần học thuộc bảng tuần hoàn không?
Không cần học thuộc toàn bộ, nhưng nên nhớ:
Các nhóm quan trọng
Vị trí tương đối của nguyên tố
Làm sao để nhớ nhanh bảng tuần hoàn?
Học theo nhóm
Kết hợp làm bài tập
Luyện đọc bảng thường xuyên
Bảng tuần hoàn hiện có bao nhiêu nguyên tố?
Hiện nay có hơn 100 nguyên tố (118 nguyên tố đã được công nhận).
Vì sao cần học bảng tuần hoàn?
Vì đây là nền tảng để:
- Hiểu tính chất hóa học
- Giải bài tập nhanh
- Học tốt các phần hóa học khác
Lời Kết
Hiểu và sử dụng thành thạo bảng tuần hoàn nguyên tố hóa học sẽ giúp bạn học tốt môn Hóa và xử lý bài tập nhanh hơn. Khi nắm được cách đọc, cấu tạo và quy luật biến đổi, bạn không cần học thuộc máy móc mà vẫn có thể suy ra tính chất của nguyên tố.
Để ghi nhớ lâu, hãy kết hợp giữa việc quan sát bảng, học theo nhóm và luyện tập thường xuyên. Chỉ cần quen cách nhìn bảng, bạn sẽ thấy việc học hóa học trở nên dễ dàng và logic hơn rất nhiều.